Մոնոկլոնալ հակամարմինային թերապիա
Մոնոկլոնալ հակամարմինային թերապիա՝ իմունոթերապիայի տեսակ, որն օգտագործվում է մոնոկլոնալ հակամարմինները որոշակի բջիջների կամ սպիտակուցների հետ կապելու նպատակով։ Թերապիայի իմաստը կայանում է նրանում, որ հիվանդի իմունիտետը ակտիվանա և ինքը սկսի ակտիվ պայքարել տվյալ բջիջների դեմ[1]։ Բոլորովին վերջերս մոնոկլոնալ հակամարմինները սկսել են օգտագործել T-ռեգուլյացիային մասնակցող յուրահատուկ մոլեկուլների հետ կապման համար։ Սա հնարավորություն է տալիս վերացնել որոշ հիվանդությունների կողմից ակտիվացող T-բջջային պատասխանի արգելակումը։ Այս պրոցեսը իմուն չեքփոինթ թերապիան է[2]։
Հնարավոր է ստեղծել mAb գրեթե բոլոր արտաբջջային կամ բջջի մակերեսին էքսպրեսվող սպեցիֆիկ թիրախի համար։ Ներկայումս կատարվում են մի շարք փորձեր, որոնք հնարավորություն կտան ստանալ հակամարմիններ այնպիսի հիվանդությունների համար, ինչպիսիք են ռևմատոիդ արթրիտը, ցրված սկլերոզը, Ալցհայմերի հիվանդությունը, Էբոլան, քաղցկեղի տարբեր տեսակներ[3]։
Հակամարմնի կառուցվածք և ֆունկցիա
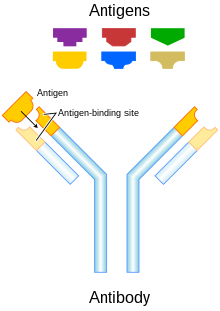
խմբագրելԻմունոգլոբուլին G (IgG) հակամարմինները հետերոդիմետրիկ մոլեկուլներ են (մոտավորապես 150կԴա)՝ կազմված ծանր և թեթև պոլիպեպտիդային շղթաներից։ Թեթև շղթաների երկու տեսակներն են կապպան (κ) և լյամբդան (λ)։ Պապաին ֆերմենտով ճեղքման արդյունքում հնարավոր է լինում հակամարմնի մոլեկուլի Fab (fragment-antigen binding) հատվածն անջատել Fc (fragment constant) հատվածից։ Fab հատվածները պարունակում են վարիաբել դոմեններ, որոնք կազմված են հակամարմնի երեք հիպերվարիաբել ամինաթթվային դոմեններից։ IgG-ի չորս հայտնի ենթատեսակները ներառված են հակամարմին կախյալ բջջային ցիտոտոքսիկության մեջ[4]։
Հակամարմինները հանդիսանում են ձեռքբերովի իմուն պատասխանի գլխավոր կոմպոնենտները, քանի որ դրանք պատասխանատու են և՛ օտար անտիգենի ճանաչման, և՛ իմուն պատասխանի ստիմուլացման համար։ Մոնոկլոնալ հակամարմինային թերապիան հնարավորություն է տալիս սինթեզել հակամարմիններ տարբեր ուռուցքային բջիջների կողմից էքսպրեսվող անտիգենների դեմ[5]։ Մոնոկլոնալ հակամարմինները կարող են անցնել իմուն համակարգ պասիվ կամ ակտիվ իմունիտետի միջոցով։
Ակտիվ մոնոկլոնալ հակամարմինային թերապիայի առավելությունը նրանում է, որ թերապիայի արդյունքում իմուն համակարգը սկսում է երկար ժամանակ արտադրել հակամարմիններ։ Բուժման ընթացքում իմուն պատասխանը որոշակի անտիգենների հանդեպ ոչ միանշանակ կարող է լինել՝ հատկապես տարեցների մոտ։ Ակտիվ մոնոկլոնալ հակամարմինային թերապիայի կողմնակի էֆֆեկտները պայմանավորված են անտիգենի դեմ երկարաժամկետ պատասխանով[6]։
Պասիվ մոնոկլոնալ հակամարմինային թերապիան հնարավորթյուն է տալիս օրգանիզմում պահպանել հակամարմինների հաստատուն կոնցենտրացիա, իսկ կողմնակի ազդեցությունների զարգացման դեպքում պետք է ուղղակի դադարեցնել բուժումը։ Այնուամենայնիվ թերապիայի կրկնումները և բարձր արժեքը հանդիսանում են մեծ թերություններ[6]։
Մոնոկլոնալ հակամարմինային թերապիան բավականին լավ արդյունք է տալիս քաղցկեղի, աուտոիմուն հիվանդությունների և նյարդային համակարգի հիվանդությունների, օրինակ Ալցհայմերի հիվանդությունը, բուժման գործում։ Քաղցկեղային բջիջները շատ արագ են պրոլիֆերացվում և ունեն յուրահատուկ մեխանիզմներ, որոնց միջոցով խուսափում են իմուն պատասխանից։ Այս դեպքում մոնոկլոնալ հակամարմինները կարող են օգնել բնածին իմունիտետին ավելի լավ ճանաչել օտար անտիգենները, քանի որ այդ հակամարմինները հաջողությամբ կապվում են քաղցկեղային բջիջների թիրախ անտիգենների հետ և ակտիվացնում իմուն համակարգը։
Պատմություն
խմբագրելԻմունոթերապիան զարգացել է հակամարմինների կառուցվածքի բացահայտումից և հիբրիդոմա տեխնոլոգիայի զարգացումից անմիջապես հետո՝ 1970-ականներին։ Հիբրիդոմա տեխնոլոգիան համարվում է մոնոկլոնալ հակամարմինների ստացման առաջին աղբյուրը[8][9]։ Այս զարգացումները հնարավորություն տվեցին թիրախավորել ուռուցքները և՛ in-vivo, և՛ in-vitro։ Չարորոակ նորագոյացություններին վերաբերող առաջին փորձերը ցույց տվեցին, որ մոնոկլոնալ հակամարմինային թերապիան հաջողում է սահմանափակ կամ կարճաժամկետ, եթե խոսքը վերաբերում է արյան չարորակացումներին[10][11]։ Թերապիան պետք է հարմարեցվեր նաև յուրաքանչյուր առանձին պացիենտի, ինչն անիրագործելի էր կլինիկական փորձարկումների պարամետրերում։
Ստեղծված հակամարմինների խմբերն էին՝ մուրինային, խիմերիկ, մարդատիպ և լիովին մարդու։ Յոորաքանչյուր խմբի հակամարմիններ ստացան յուրահատուկ տարբերակիչ վերջավորություններ։
Մուրին
խմբագրելԱռաջին թերապևտիկ հակամարմինները մուրինի անալոգներ էին (վերջավորությունը -omab)։ Այս հակամարմինները ունեն in vivo կարճ կյանք՝ պայմանավորված իմուն կոմպլեքսների ձևավորմամբ, ուռուցքի մեջ թափանցելու սահմանափակ հնարավորություններ և բնութագրվում են տիրոջ օրգանիզմի իմուն էֆֆեկտոր ֆունկցիաների ոչ ադեկվատ ակտիվացմամբ[12]։ Հետագայում խիմերիկ և մարդատիպ հակամարմինները փոխարինեցին մուրինային հակամարմիններին[13]։
Մուրինային հակամարմինները սկզբում ստանում էին հիբրիդոմա տեխնոլոգիայով, սակայն մուրինի և մարդու իմուն համակարգի անհամապատասխանությունները բերեցին այս հակամարմինների կլինիկական ձախողման։ Մուրինային հակամարմինների մեծ թերությունն այն էր, որ դրանք նվազեցնում էին ցիտոտոքսիկության ստիմուլյացիան և կոմպլեքսների ձևավորումը, որն էլ բերում էր ալերգիկ ռեակցիաների զարգացման՝ նույնիսկ անաֆիլակտիկ շոկի[12]։ Ժամանակի ընթացքում հիբրիդոմա տեխնոլոգիան փոխարինվեց ԴՆԹ կլոնավորման տեխնոլոգիայով, տրանսգենային մկներով և ֆագային դիսփլեյով[13]։
Խիմերիկ և մարդատիպ
խմբագրելՈրպեսզի իջեցվեր մուրինի իմունոգենությունը (իմուն համակարգի պայքարը հակամարմնի դեմ), մուրինի մոլկուլից հանվեցին իմունոգեն պարունակությունը և բարձրացվեց իմունոլոգիական արդյունավետությունը[12]։ Այսպես ստեղծվեցին խիմերիկ (վերջավորությունը -ximab) և մարդատիպ (վերջավորությունը -zumab) հակամարմինները։ Խիմերիկ հակամարմինները կազմված ենն մուրինի մոլեկուլի վարիաբել հատվածներից, որոնք միացված են մարդու հակամարմնի կոնստանտ հատվածներին։ Այս հակամարմինները մոտ 65%-ով մարու են, քանի որ կազմված են մարդու գենի կապպա թեթև շղթայից և IgG1 ծանր շղթայից։ Այսպիսով նվազում է իմունոգենությունը և բեարձրանում է շիճուկի կյանքի ժամանակը։
Մարդատիպ հակամարմինները ստանում են մուրինի հիպերվարիաբել հատվածները մարդու հակամարմնի ամինաթթվային դոմեններին միացնելու արդյունքում։ Այսպիսով ստացված մոլեկուլը 95%-ով մարդկային ծագում ունի։ Մարդատիպ հակամարմիններն ավելի թույլ են կապվում թիրախին քան մուրինային հակամարմինները, ինչը բերում է հարյուրավոր անգամներ աֆինության նվազման[14][15]։ Հակամարմին-անտիգեն կապի ուժեղացումը հնարավոր դարձավ կոմպլիմենտարությունը որոշող տեղեմասերում մուտացացիաների առաջացումով[16]։ Մուտացիաներն առաջացնելու համար օգտագործվեցին շղթաների տեղափոխում, կոմպլիմենտարությունը որոշող տեղեմասերի ռանդոմիզացիա, ՊՇՌ, E. coli մոտատոր շտամներ և սայտ-սփեցիֆիկ մուտագենեզ մեխանիզմները[1]։
Մարդու մոնոկլոնալ հակամարմիններ
խմբագրելՄարդու մոնոկլոնալ հակամարմինները (վերջավորությունը -umab) սինթեզվում են տրանսգենային մկներից կամ ֆագային դիսփլեյից՝ մարդու իմոնոգլոբուլինային գեները մուրինի գենոմի մեջ անցկացնելով և տրանսգենային մկանը ցանկալի անտիգենի դեմ պատվաստելու միջոցով։ Պատվաստումից հետո մկան իմուն համակարգը սկսում է արտադրել մոնոկլոնալ հակամարմինները[13]։ Այսպիսով մկան հակամարմինները in-vitro տրանսֆորմացվում են մարդու հակամարմինների[5]։
Մարդու IgG հակամարմնի ծանր և թեթև շղթաները էքսպրեսվում են կառուցվածքային պոլիմորֆ (ալոտիպ) ձևով։ Մարդու IgG ալոտիպը հնարավոր է բերի իմունոգենության[17][18]։
Թիրախ հիվանդություններ
խմբագրելՔաղցկեղ
խմբագրելՄոնոկլոնալ հակամարմինային թերապիան հնարավորթյուն է տալիս տարբեր մեխանիզմներով թիրախավորել քաղցկեղային բջիջները։ Ռամուցիրումաբը ռեկոմբինանտ մարդու մոնոկլոնալ հակամարմին է, որն օգտագործվում է չարորակ նորագոյացությունների բուժման համար[19]։ Փորձերը ցույց են տվել, որ հակամարմնիային թերապիան բավականին լավ արդյունք է տալիս մանկական լիմֆոմայի բուժման գործում[20]։
Աուտոիմուն հիվանդություններ
խմբագրելԻնֆլիքսիմաբը և ադալիմումաբը մեծապես օգտագործվում են ռևմատոիդ արթրիտի, Կրոնի հիվանդության և ոչ սպեցիֆիկ խոցային կոլիտի բուժման համար։ Այս թերապևտիկ մոնոկլոնալ հակամարմինները ազդում են աուտոիմուն հիվանդությունների զարգացման վրա, քանի որ կապվում են TNF-α-ի հետ[21]։ Բազիլիքսիմաբը և դացիլիզումաբը արգելակում են ակտիվ T-բջիջների կողմից էքսպերսվող IL-2-ը՝ խոչընդոտելով երիկամային տրանսպլանտանտի մերժումը[21]։ Օմալիզումաբը օգտակար է չափավոր կամ ծանր ալերգիկ ասթմայի դեպքում, քանի որ արգելակում է մարդու իմունոգլոբուլին E-ն (IgE)։
Ալցհայմերի հիվանդություն
խմբագրելԱլցհայմերի հիվանդությունը բազմակողմանի, տարիքից կախված, պրոգրեսիվող նեյրոդեգեներատիվ հիվանդություն է։ Հանդիսանում է դեմենցիայի զարգացման գլխավոր պատճառներից մեկը[22]։ Համաձայն ամիլոիդային տեսության տեղի է ունենում արտաբջջային բետա ամիլոիդի կուտակում, որը բերում է սինապտիկ դիսֆունկցիայի և նեյրոդեգեներացիայի[23]։ Մոնոկլոնակ հակամարմիններով բուժումը դրոնկան արդյունք է ցուցաբերում հիվանդության բուժման գործում, քանի որ արգելակում է Aβ-օլիգոմերիզացիան և կանխում նեյրոտոքսիկությունը։ Հետաքրքիր է այն փաստը, որ mAb-երը բավականին մեծ են և չեն կարող անցնել արյուն-ուղեղային պատնեշի պասիվ պրոտեինային անցուղիներով։ Սակայն համաձայն ծայրամասային հոսքի վարկածի mAb-երը կարիք չունեն անցելու արյուն-ուղեղային պատնեշը[24]։ Այնուամենայնիվ մի շարք Ալցհայմերի հիվանդության բուժման փորձեր ձախողվել են[23]։
Հակա-Aβ վակցինաները կարող են ակտիվացնել APP (amyloid precursor proteins) ունեցող տրանսգենային մկների մոտ հակամարմին կախյալ Aβ ագրեգատների մաքրումը և նվազեցնել կոգնիտիվ խանգարումների զարգացման ռիսկը[22]։ Վակցինաները ստիմուլացնում են իմուն համակարգը և այն սկսում է արտադրել իր սեփական հակամարմինները[25]։ Այսպես տրանսգենային մկների մոտ աշխատում է ակտիվ իմունիզացիան։ Հնարավոր է նաև կենդանու օրգանիզմ ներմուծել պատրաստի հակամարմիններ, այսինքն կատարել պասիվ իմունիզացիա։ APP ունեցող մկների դեպքում և՛ պասիվ, և՛ ակտիվ իմունիզացիան տվել են դրական արդյունքներ Aβ ագրեգատների մաքրման և կոնգնիտիվ ֆունկցիայի վերականգնման հարցում[23]։ Ներկայումս կատարվում են փորձեր Ալցհայմերը բուժելու և՛ պասիվ, և՛ ակտիվ իմունիզացիայի միջոցով։ Այս փորձերը հաստատված են ՍԴՎ-ի կողմից, և հավանաբար մոտակա ժամանակներում կհրապարակվեն արդյունքները[23]։ Փորձարկումների փուլում են նաև բապինեյզումաբ, սոլանեզումաբ և գաուտեներումաբ դեղերը։
Բապինեյզումաբ
խմբագրելԲապինեյզումաբը մարդատիպ հակա-Aβ մոնոկլոնալ հակամարմին է՝ ուղղված Aβ-ի N- վերջավորության դեմ։ Երկրորդ ֆազայի փորձերը ցույց են տվել, որ հակամարմինը իջեցնում է Aβ ագրեգատների քանակությունը չափավոր կամ թեթև ընթացով Ալցհայմերի հիվանդություն ունեցող պացիենտների մոտ։ Սակայն մեծ քանակներով ապոլիպոպրոտեին (APOE) e4 ունեցող պացիենտների մոտ բապինեյզումաբը բերում է ցիտոտոքսիկ վիճակի՝ վազոգենային այտուցի[26]։ Այտուցն առաջանում է, քանի որ վնասվում է արյուն ուղեղային պատնեշը և տեղի է ունենում մազանոթներից հեղուկի անցում ուղեղի ներբջջային և արտաբջջային տարածություններ[27]։ Երրորդ ֆազայի փորձերի արդյունքում պարզ է դարձել, որ APOE e4 բարձր և APOE e4 ցածր մակարդակով պացիենտների մոտ բապինեյզումաբը էական կերպով չի ազդել Aβ ագրեգատների քանակի վրա։ Այդ է պատճառը, որ բապինեյզումաբին վերաբերող փորձերը դադարեցվել են[27]։
Սոլանեզումաբ
խմբագրելՍոլանեզումաբը հակա-Aβ մոնոկլոնալ հակամարմին է՝ ուղղված Aβ-ի N- վերջավորության դեմ։ Առաջին և երկրորդ ֆազայի փորձերի ընթացքում սոլանեզումաբով բուժումը բերել է ուղեղ-ողնուղեղային հեղուկում Aβ-ի մակարդակի բարձրացման, հետևաբար գլխուղեղում նվազել են Aβ ագրեգատները։ Բացի այդ, չեն հայտնաբերվել կողմնակի էֆֆեկտներ։ Երրորդ ֆազայի փորձերում սոլանեզումաբով բուժումը թեթև ընթացքով պացիենտների մոտ հանգեցրել է կոգնիտիվ վնասումների վերացման, իսկ ծանր ընթացքով հիվանդենրի մոտ էական փոփոխություններ չեն հայտնաբերվել։ Այնուամենայնիվ, Aβ կոնցենտրացիան էապես չի փոխվել ՝ AD այլ բիոմարկերների հետ միասին, ներառյալ ֆոսֆո-տաու էքսպրեսիան և հիպոկամպի ծավալը։ III ֆազայի փորձարկումները ներկայումս շարունակվում են[24]։
Կանխարգելիչ փորձեր
խմբագրելԵրրորդ ֆազայի փորձերում մի շարք դեղերի ձախողումը հանգեցրեց Ալցհայմների հիվանդությունը կանխարգելոլու միջոցների որոնման։ Պասիվ հակա-Aβ թերապաին հնարավոր է օգտագործել հիվանդության զարգացումը կանխելու և ծանր բարդություններից խուսափելու համար։ Ներկայումս կատարվում են փորձեր տարեցների և գենետիկ նախատրամադրվածություն ունեցող հիվանդների մոտ հիվանդության կանխարգելման ուղղությամբ։ Այդ փորձերն են՝ Alzheimer's Disease (A4), the Alzheimer's Prevention Initiative (API), and DIAN-TU[24]։ DIAN-TU-ն մեկնարկել է 2012-ին։ Այն կենտրոնանում է Ալցհյմերի հիվանդության գենային նախատրամադրվածություն ունեցող երիտասարդ անձանց վրա[24]։ A4 փորձերը կենտրոնանում են այն տարեց անձանց վրա, ովքեր չունեն գենետիկ նախատրամադրվածություն[24]։
Թերապիայի տեսակներ
խմբագրելՌադիոիմունոթերապիա
խմբագրելՌադիոիմունոթերապիան օգտագործում է ռադիոակտիվորեն կոնյուգացված մուրինային հակամարմիններ, որոնք ակտիվ են բջջային անտիգենների դեմ։ Փորձերը հիմնականում կատարվում լիմֆոմաների ուղղությամբ, քանի որ դրանք զգայուն են ճառագայթման հանդեպ։ Չափից դուրս ճառագայթումից խուսափելու համար ընտրվել են մուրինային հակամարմինները, քանի որ դրանք ունեն բարձր իմունոգենություն և արագ են վերացնում քաղցկեղային բջիջները։ Ոչ հոջկինյան լիմֆոմայի բուժման համար օգտագործվում է տոզիտումոմաբը։
Հակամարմին ուղղված նախադեղային թերապիա
խմբագրելՀակամարմին ուղղված նախադեղային թերապիան օգտագործում է քաղցկեղի դեմ ազդող մոնոկլոնալ հակամարմիններ՝ կապված դեղին ակտիվացնող ֆերմենտի հետ։ Ոչ թունավոր հակամարմնի կանոնավոր ներմուծումը բերում է օրգանիզմում թոքսիկի փոխակերպման՝ հանգեցնելով ցիտոտոքսիկ էֆֆեկտի զարգացման և քաղցկեղային բջջի ոչնչացման։ Այս թերապիայի կլինիկական հաջողությունները սահմանափակ են[28]։
Հակամարմին-դեղ կոնյուգատներ
խմբագրելՀակամարմին-դեղ կոնյուգատները հակամարմիններ են, որոնք կապված են մեկ կամ մի քանի դեղի մոլեկուլի հետ։ Աշխատանքի մեխանիզմը հետևյալն է․ հակամարմինի միջոցով կոնյուգատը հասնում է թիրախին, տեղի է ունենում դեղի առանձնացում հակամարմինից և դեղի միջոցով թիրախի ոչնչացում։ Ներկայումս հակամարմին-դեղ կոնյուգատները փորձարկումների փուլում են։ 2016-ին դրանցից որոշները հաստատվել են։
Իմունոլիպոսոմային թերապիա
խմբագրելԻմունոլիպոսոմները իրենցից ներկայացնում են հակամարմնին միացված լիպոսոմներ։ Լիպոսոմները կարող են տեղափոխել դեղեր կամ թերապևտիկ նուկլեոտիդներ և մոնոկլոնալ հակամարմինների հետ կապելու դեպքում կարող են օգտագործվել չարորակ բջիջների դեմ։ Իմունոլիպոսոմները հաջողության են հասել in-vivo։ Օգտագործվել են մարդու տրանսֆերին ընկալիչի դեմ սինթեզված հակամարմիններ։ Իմունոլիպոսոմը, հասնելով քաղցկեղին, բջիջների մեջ ներդնում է քաղցկեղ ճնշող գեներ, որոնք ակտիվանալով բերում են բջջի ոչնչացման։ Կրծքագեղձի քաղցկեղի և գլխուղեղի քաղցկեղի բուժման նպատակով կիրառվել են իմունոլիպոսոմներ, որոնք ներդնում են բջիջների մեջ հյուսվածք-սպեցիֆիկ գեներ[29]։
Չեքփոինթ թերապիա
խմբագրելՉեքփոինթ թերապիան օգտագործում է հակամարմիններ և այլ միջոցներ, որոնց միջոցով արգելակում է քաղցկեղային բջիջների կողմից իմուն համակարգի սուպրեսիան։ Քաղցկեղային բջջի յուրաքանչյուր պաշտպանական կետ անվանում են չեքփոինթ։ Համակցված թերապիան կարող է ճնշել միանգամից մի քանի պաշտպանական կետ։ Հայտնի են CTLA-4 ուղղված իպիլիմումաբը, PD-1 ուղղված նիվոլումաբը, պեմբրոլիզումաբը[2]։
Ուռուցքային միկրոշրջապատը կանխում է T-բջիջների անցոմը ուռուցքի մեջ։ Օգտագորվող մեխանիղմներից է CCL2 քեմոկինի նիտրացումը և T-բջիջների ստրոմայում թակարդումը։ Մետամիելոցիտային և քաղցկեղային բջիջները կորղ են up-regulation-ի ենթարկել PD-L1 էքսպրեսիան, որը պայմանավորված է հիպօքսիկ վիճակով կամ յուրահատուկ ցիտոկինների արտադրությամբ (IFNβ)[30]։
ՍԴՎ հաստատված թերապևտիկ հակամարմիններ
խմբագրելՍննդի և դեղերի վարչության կողմից առաջին հատատված մոնոկլոնալ հակամարմինը մուրին IgG2a CD3 սպեցիֆիկ տրանսպլանտատի մերժման դեմ կիրառվող OKT3-ն էր (այլ կերպ Մուրոմոնաբ)։ Այս մոնոկլոնալ հակամարմինը օգտագործվում էր այն պացիենտների շրջանում, ովքեր ստերոիդ ռեզիստենտ էին[31]։
| Հակամարմին | Բրենդային անվանում | Կազմակեր-պություն | Հաստատման տարեթիվ | Ընդունման եղանակ | Տեսակ | Թիրախ | Ցուցում
(թիրախ հիվանդություն) |
BLA STN | Դեղի
պիտակ |
|---|---|---|---|---|---|---|---|---|---|
| Աբցիքսիմաբ | ReoPro | Centocor | 12/22/1994 | ներերակային | Խիմերիկ Fab | GPIIb/IIIa | Միջմաշկային կորոնար միջամտություն | 103575 | Link |
| Ադալիմումաբ | Humira | Abbvie | 12/31/2002 | ենթամաշկային | լիովին մարդու | TNF | Ռևմատոիդ արթրիտ | 125057 | Link |
| Ադալիմումաբ-ատտո | Amjevita | Amgen | 9/23/2016 | ենթամաշկային | լիովին մարդու, բիոանալոգ | TNF | Ռևմատոիդ արթրիտ Յուվենիլ իդեոպաթիկ արթրիտ Փսորիատիկ արթրիտ Անկիլոզացնող սպոնդիլոարթրիտ Կրոնի հիվանդություն Ոչ սպեցիֆիկ խոցային կոլիտ |
761024 | Link |
| Ադո-տրանստուզումաբ | Kadcyla | Genentech | 2/22/2013 | ներերակային | մարդատիպ, հակամարմին-դեղ կոնյուգատ | HER2 | Մետաստատիկ կրծքագեղձի քաղցկեղ | 125427 | Link |
| Ալեմտուզումաբ | Campath, Lemtrada | Genzyme | 5/7/2001 | ներերակային | մարդատիպ | CD52 | Քրոնիկ լիմֆոցիտային լեյկեմիա | 103948 | Link |
| Ալիրոկումաբ | Praluent | Sanofi Aventis | 7/24/2015 | ենթամաշկային | լիովին մարդու | PCSK9 | Հետերոզիգոտ ընտանեկան հիպերխոլեստերոլեմիա familial hypercholesterolemia Ռեֆրակտոր հիպերխոլեստերոլեմիա |
125559 | Link |
| Ատեզոլիզումաբ | Tecentriq | Genentech | 5/18/2016 | ներերակային | մարդատիպ | PD-L1 | Ուրոթելիալ կարցինոմա | 761034 | Link |
| Ատեզոլիզումաբ | Tecentriq | Genentech | 10/18/2016 | ներերակային | մարդատիպ | PD-L1 | Ուրոթելիալ կարցինոմա Թոքի ոչ մանր բջջային քաղցկեղ |
761041 | Link |
| Ավելումաբ | Bavencio | EMD Serono | 3/23/2017 | ներերակային | լիովին մարդու | PD-L1 | Մերկելի բջջային քաղցկեղ | 761049 | Link |
| Բազիլիքսիմաբ | Simulect | Novartis | 5/12/1998 | ներերակային | խիմերիկ | IL2RA | երիկամային տրանսպլանտանտի մերժման կանխում | 103764 | Link |
| Բելիմումաբ | Benlysta | Human Genome Sciences | 3/9/2011 | ներերակային | լիովին մարդու | BLyS | Համակարգային կարմիր գայլախտ | 125370 | Link |
| Բևացիզումաբ | Avastin | Genentech | 2/26/2004 | ներերակային | մարդատիպ | VEGF | Կոլոռեկտալ քաղցկեղ | 125085 | Link |
| Բեզլոտոքսումաբ | Zinplava | Merck | 10/21/2016 | ներերակային | լիովին մարդու | Clostridium difficile տոքսին B | Հետադարձ Clostridium difficile վարակի կանխում | 761046 | Link |
| Բլինատումոմաբ | Blincyto | Amgen | 12/3/2014 | ներերակային | մկան, բիսպեցիֆիկ | CD19 | Պրեկուրսոր B-բջջային սուր լիմֆոբլաստիկ լեյկեմիա | 125557 | Link |
| Բրենտուքսիմաբ վեդոտին | Adcetris | Seattle Genetics | 9/19/2011 | ներերակային | խիմերիկ, հակամարմին-դեղ կոնյուգատ | CD30 | Հոջկինի լիմֆոմա Անապլաստիկ հսկա բջջային լիմֆոմա |
125388 | Link |
| Բրոդալումաբ | Siliq | Valeant | 2/15/2017 | ենթամաշկային | խիմերիկ | IL17RA | Փսորիազ | 761032 | Link |
| Կանակինումաբ | Ilaris | Novartis | 6/17/2009 | ենթամաշկային | լիովին մարդու | IL1B | Կրիոպրին-ասոցացված համակարգային համախտանիշ | 125319 | Link |
| Կապրոմաբ պենդետիդ | ProstaScint | Cytogen | 10/28/1996 | ներերակային | մուրին, ռադիոակտիվ նշված | PSMA | Նոր ախտորոշված շագանակագեղձի քաղցկեղի կամ հետպրոստատէկտոմիայի ախտորոշիչ պատկերապատման միջոց | 103608 | Link |
| Ցերտոլիզումաբ պեգոլ | Cimzia | UCB (company) | 4/22/2008 | ենթամաշկային | մարդատիպ | TNF | Կրոնի հիվանդություն | 125160 | Link |
| Ցետուքսիմաբ | Erbitux | ImClone Systems | 2/12/2004 | ներերակային | խիմերիկ | EGFR | Կոլոռեկտալ կարցինոմա | 125084 | Link |
| Դակլիզումաբ | Zenapax | Roche | 12/10/1997 | ներերակային | մարդատիպ | IL2RA | երիկամային տրանսպլանտանտի մերժման կանխում | 103749 | Link |
| Դակլիզումաբ | Zinbryta | Biogen | 5/27/2016 | ենթամաշկային | մարդատիպ | IL2R | Ցրված սկլերոզ | 761029 | Link |
| Դարատումումաբ | Darzalex | Janssen Biotech | 11/16/2015 | ներերակային | լիովին մարդու | CD38 | Բազմակի միելոմա | 761036 | Link Արխիվացված 2018-05-14 Wayback Machine |
| Դենոսումաբ | Prolia, Xgeva | Amgen | 6/1/2010 | ենթամաշկային | լիովին մարդու | RANKL | Օստեոպորոզ պոստմենոպաուզալ շրջանում գտնվող կանանց մոտ | 125320 | Link |
| Դինուտուքսիմաբ | Unituxin | United Therapeutics | 3/10/2015 | ներերակային | խիմերիկ | GD2 | Մանկական նեյրոբլաստոմա | 125516 | Link |
| Դուպիլումաբ | Dupixent | Regeneron Pharmaceuticals | 3/28/2017 | ենթամաշկային | լիովին մարդու | IL4RA | Ատոպիկ դերմատիտ, ասթմա | 761055 | Link |
| Դուրվալումաբ | Imfinzi | AstraZeneca | 5/1/2017 | ներերակային | լիովին մարդու | PD-L1 | Ուրոթելիալ քաղցկեղ | 761069 | Link |
| Էկուլիզումաբ | Soliris | Alexion | 3/16/2007 | ներերակային | մարդատիպ | Կոմպլիմենտի համակարգի C5 | Պարոքսիզմալ գիշերային հեմոգլոբինուրիա | 125166 | Link |
| Էլոտուզումաբ | Empliciti | Bristol-Myers Squibb | 11/30/2015 | ներերակային | մարդատիպ | SLAMF7 | Բազմակի միելոմա | 761035 | Link |
| Էվոլոկումաբ | Repatha | Amgen | 8/27/2015 | ենթամաշկային | լիովին մարդու | PCSK9 | Հետերոզիգոտ ընտանեկան հիպերխոլեստերոլեմիա familial hypercholesterolemia Ռեֆրակտոր հիպերխոլեստերոլեմիա |
125522 | Link |
| Գոլիմումաբ | Simponi | Centocor | 4/24/2009 | ենթամաշկային | լիովին մարդու | TNF | Ռևմատոիդ արթրիտ Փսորիատիկ արթրիտ Անկիլոզացնող սպոնդիլոարթրիտ |
125289 | Link |
| Գոլիմումաբ | Simponi Aria | Janssen Biotech | 7/18/2013 | ներերակային | լիովին մարդու | TNF | Ռևմատոիդ արթրիտ | 125433 | Link |
| Իբրիտումոմաբ տիուքսետան | Zevalin | Spectrum Pharmaceuticals | 2/19/2002 | ներերակային | մուրին, ռադիոիմունոթերապիա | CD20 | Ֆոլիկուլյար կամ ոչ Հոջկինյան լիմֆոմա | 125019 | Link |
| Իդարուցիզումաբ | Praxbind | Boehringer Ingelheim | 10/16/2015 | ներերակային | մարդատիպ Fab | Դաբիգատրան | Դաբիգատրանի հակամակարդիչ էֆֆեկտի հրատապ վերացում | 761025 | Link |
| Ինֆլիքսիմաբ | Remicade | Centocor | 8/24/1998 | ներերակային | խիմերիկ | TNF alpha | Կրոնի հիվանդություն | 103772 | Link |
| Ինֆլիքսիմաբ-abda | Renflexis | Samsung Bioepis | 4/21/2017 | ներերակային | խիմերիկ, բիոանալոգ | TNF | Ռևմատոիդ արթրիտ Փսորիատիկ արթրիտ Անկիլոզացնող սպոնդիլոարթրիտ Կրոնի հիվանդություն Ոչ սպեցիֆիկ խոցային կոլիտ |
761054 | Link |
| Ինֆլիքսիմաբ-dyyb | Inflectra | Celltrion Healthcare | 4/5/2016 | ներերակային | խիմերիկ, բիոանալոգ | TNF | Ռևմատոիդ արթրիտ Յուվենիլ իդեոպաթիկ արթրիտ Փսորիատիկ արթրիտ Անկիլոզացնող սպոնդիլոարթրիտ Կրոնի հիվանդություն Ոչ սպեցիֆիկ խոցային կոլիտ |
125544 | Link |
| Իպիլիմումաբ | Yervoy | Bristol-Myers Squibb | 3/25/2011 | ներերակային | լիովին մարդու | CTLA-4 | Մետաստատիկ մելանոմա | 125377 | Link |
| Իքսեկիզումաբ | Taltz | Eli Lilly | 3/22/2016 | ենթամաշկային | լիովին մարդու | IL17A | Փսորիազ | 125521 | Link |
| Մեպոլիզումաբ | Nucala | GlaxoSmithKline | 11/4/2015 | ենթամաշկային | լիովին մարդու | IL5 | Ծանր ասթմա | 125526 | Link |
| Նատալիզումաբ | Tysabri | Biogen Idec | 11/23/2004 | ներերակային | մարդատիպ | alpha-4 ինտեգրին | Ցրված սկլերոզ | 125104 | Link |
| Նեցիտումումաբ | Portrazza | Eli Lilly | 11/24/2015 | ներերակային | լիովին մարդու | EGFR | Թոքի ոչ մանր տափակ բջջային քաղցկեղ | 125547 | Link |
| Նիվոլումաբ | Opdivo | Bristol-Myers Squibb | 12/22/2014 | ներերակային | լիովին մարդու | PD-1 | Մետաստատիկ մելանոմա | 125554 | Link |
| Նիվոլումաբ | Opdivo | Bristol-Myers Squibb | 3/4/2015 | ներերակային | լիովին մարդու | PD-1 | Թոքի ոչ մանր տափակ բջջային քաղցկեղ | 125527 | Link |
| Օբիլտոքսաքսիմաբ | Anthem | Elusys Therapeutics | 3/18/2016 | ներերակային | խիմերիկ | Սիբիրախտի տոքսինի պաշտպանիչ անտիգեն | Սիբիրախտ | 125509 | Link |
| Օբինուտուզումաբ | Gazyva | Genentech | 11/1/2013 | ներերակային | մարդատիպ | CD20 | Քրոնիկ լիմֆոցիտային լեյկեմիա | 125486 | Link |
| Օկրելիզումաբ | Ocrevus | Genentech | 3/28/2017 | ներերակային | մարդատիպ | CD20 | Ցրված սկլերոզ | 761053 | Link |
| Օֆատումումաբ | Arzerra | Glaxo Grp | 10/26/2009 | ներերակային | լիովին մարդու | CD20 | Քրոնիկ լիմֆոցիտային լեյկեմիա | 125326 | Link |
| Օլարատումաբ | Lartruvo | Eli Lilly | 10/19/2016 | ներերակային | լիովին մարդու | PDGFRA | Փափուկ հյուսվածքի սարկոմա | 761038 | Link |
| Օմալիզումաբ | Xolair | Genentech | 6/20/2003 | ենթամաշկային | մարդատիպ | IgE | Չափավոր կամ ծանր պերսիստող ասթմա | 103976 | Link |
| Պալիվիզումաբ | Synagis | MedImmune | 6/19/1998 | միջմկանային | մարդատիպ | Ռեսպիրատոր սինցիցիալ վիրուսի F պրոտեին | Ռեսպիրատոր սինցիցիալ վիրուս | 103770 | Link |
| Պանիտումումաբ | Vectibix | Amgen | 9/27/2006 | ներերակային | լիովին մարդու | EGFR | Կոլոռեկտալ քաղցկեղ | 125147 | Link |
| Պեմբրոլիզումաբ | Keytruda | Merck | 9/4/2014 | ներերակային | մարդատիպ | PD-1 | Մետաստատիկ մելանոմա | 125514 | Link |
| Պերտուզումաբ | Perjeta | Genentech | 6/8/2012 | ներերակային | մարդատիպ | HER2 | Կրծքագեղձի քաղցկեղ | 125409 | Link |
| Ռամուցիրումաբ | Cyramza | Eli Lilly | 4/21/2014 | ներերակային | լիովին մարդու | VEGFR2 | Ստամոքսի քաղցկեղ | 125477 | Link |
| Ռանիբիզումաբ | Lucentis | Genentech | 6/30/2006 | աչքի մեջ ներարկում | մարդատիպ | VEGFR1 VEGFR2 |
Մակուլոդեգեներացիա | 125156 | Link |
| Ռաքսիբակումաբ | Raxibacumab | Human Genome Sciences | 12/24/2012 | ներերակային | լիովին մարդու | Bacillus anthracis-ի պաշտպանիչ անտիգեն | Սիբիրախտ | 125349 | Link |
| Ռեսլիզումաբ | Cinqair | Teva | 3/23/2016 | ներերակային | մարդատիպ | IL5 | Ծանր ասթմա | 761033 | Link |
| Ռիտուքսիմաբ | Rituxan | Genentech | 11/26/1997 | ներերակային | խիմերիկ | CD20 | Ոչ հոջկինյան լիմֆոմա | 103705 | Link |
| Սեկուկինումաբ | Cosentyx | Novartis | 1/21/2015 | ենթամաշկային | լիովին մարդու | IL17A | Փսորիազ | 125504 | Link |
| Սիլտուքսիմաբ | Sylvant | Janssen Biotech | 4/23/2014 | ներերակային | խիմերիկ | IL6 | Կաստելմանի հիվանդություն | 125496 | Link |
| Տոցիլիզումաբ | Actemra | Genentech | 1/8/2010 | ներերակային | մարդատիպ | IL6R | Ռևմատոիդ արթրիտ | 125276 | Link |
| Տոցիլիզումաբ | Actemra | Genentech | 10/21/2013 | մարդատիպ | IL6R | Ռևմատոիդ արթրիտ Պոլիարտիկուլյար Յուվենիլ իդեոպաթիկ արթրիտ Համակարգային Յուվենիլ իդեոպաթիկ արթրիտ |
125472 | Link | |
| Տրանստուզումաբ | Herceptin | Genentech | 9/25/1998 | ներերակային | մարդատիպ | HER2 | Կրծքագեղձի քաղցկեղ | 103792 | Link |
| Ուստեկինումաբ | Stelara | Centocor | 9/25/2009 | ենթամաշկային | լիովին մարդու | IL12 IL23 |
Փսորիազ | 125261 | Link |
| Ուստեկինումաբ | Stelara | Janssen Biotech | 9/23/2016 | ենթամաշկային և ներերակային | լիովին մարդու | IL12 IL23 |
Փսորիազ | 761044 | Link |
| Վեդոլիզումաբ | Entyvio | Takeda | 5/20/2014 | ներերակային | մարդատիպ | Ինտեգրինային ընկալիչ | Ոչ սպեցիֆիկ խոցային կոլիտ Կրոնի հիվանդություն |
125476 | Link |
| Սարիլումաբ | Kevzara | Sanofi Aventis | 5/22/17 | ենթամաշկային | լիովին մարդու | IL6R | Ռևմատոիդ արթրիտ | 761037 | Link |
| Ռիտուքսիմաբ և | Rituxan Hycela | Genentech | 6/22/17 | ենթամաշկային | խիմերիկ, համաձևված | CD20 | Ֆոլիկուլյար լիմֆոմա Դիֆուզ հսկա B-բջջային լիմֆոմա |
761064 | Link |
| Գուսելկումաբ | Tremfya | Janssen Biotech | 7/13/17 | ենթամաշկային | լիովին մարդու | IL23 | Փսորիազ | 761061 | Link |
| Ինոտուզումաբ օզոգամիցին | Besponsa | Wyeth | 8/17/17 | ներերակային | մարդատիպ, հակամարմին-դեղ կոնյուգատ | CD22 | Պրեկուրսոր B-բջջային սուր լիմֆոբլաստիկ լեյկեմիա | 761040 | Link |
| Ադալիմումաբ-adbm | Cyltezo | Boehringer Ingelheim | 8/25/17 | ենթամաշկային | լիովին մարդու, բիոանալոգ | TNF | Ռևմատոիդ արթրիտ Յուվենիլ իդեոպաթիկ արթրիտ Փսորիատիկ արթրիտ Անկիլոզացնող սպոնդիլոարթրիտ Կրոնի հիվանդություն Ոչ սպեցիֆիկ խոցային կոլիտ |
761058 | Link |
| Գեմտուզումաբ օզոգամիցին | Mylotarg | Wyeth | 9/1/17 | ներերակային | մարդատիպ, հակամարմին-դեղ կոնյուգատ | CD33 | Սուր միելոիդ լեյկեմիա | 761060 | Link |
| Բևացիզումաբ-awwb | Mvasi | Amgen | 9/14/17 | ներերակային | մարդատիպ, բիոանալոգ | VEGF | Կոլոռեկտալ քաղցկեղ Ոչ տափակաբջջային ոչ մանր բջջային քաղցկեղ |
761028 | Link |
| Բենրալիզումաբ | Fasenra | Astrazeneca | 11/14/17 | ենթամաշկային | մարդատիպ | ինտերլեյկին-5 ընկալիչի ալֆա ենթամիավոր | Էոզինոֆիլային ֆենոտիպով ասթմա | 761070 | Link |
| Էմիցիզումաբ-kxwh | Hemlibra | Genentech | 11/16/17 | ենթամաշկային | մարդատիպ, բիսպեցիֆիկ | IXa գործոն, X գործոն | Հեմոֆիլիա A | 761083 | Link |
| Տրաստուզումաբ-dkst | Ogivri | Mylan | 12/1/17 | ներերակային | մարդատիպ, բիոանալոգ | HER2 | HER2-գերէսպրեսիայով կրծքագեղձի քաղցկեղ | 761074 | Link |
| Ինֆլիքսիմաբ-gbtx | Ixifi | Pfizer | 12/13/17 | ներերակային | խիմերիկ, բիոանալոգ | TNF | Ռևմատոիդ արթրիտ Փսորիատիկ արթրիտ Անկիլոզացնող սպոնդիլոարթրիտ Կրոնի հիվանդություն Ոչ սպեցիֆիկ խոցային կոլիտ |
761072 | Link |
| Իբալիզումաբ-uiyk | Trogarzo | TaiMed Biologics | 3/6/18 | ներերակային | մարդատիպ | CD4 | ՄԻԱՎ | 761065 | Link |
| Տիլդրակիզումաբ-asmn | Ilumya | Merck | 3/20/18 | ենթամաշկային | մարդատիպ | IL23 | Փսորիազ | 761067 | Link |
| Բուրոսումաբ-twza | Crysvita | Ultragenyx | 4/17/18 | ենթամաշկային | լիովին մարդու | FGF23 | X-շղթայակցված հիպոֆոսֆատեմիա | 761068 | Link |
| Էրենումաբ-aooe | Aimovig | Amgen | 5/17/18 | ենթամաշկային | լիովին մարդու | CGRP ռեցեպտոր | Միգրենի կանխարգելում | 761077 | Link |
Բիսպեցիֆիկ հակամարմինները, որոնք թերապևտիկ հակամարմինների ավելի նոր տարրատեսակն են, ցույց են տվել բավականին խոստումնալից արդյունքներ[32][33]։
Էկոնոմիկա
խմբագրելՍկսած 2000 թ․-ից, մոնոկլոնալ հակամարմինների պահանջարկը աճ է գրանցել։ 2006թ․-ի մոնոկլոնալ հակամարմինների մեծ հնգյակը կազմում էին բևացիզումաբը, տրաստուզումաբը, ադալիմումաբը, ինֆլիքսիմաբը և ռիտուքսիմաբը։ Այս մոնոկլոնալ հակամարմիններն օգտագործվում էին աուտոիմուն և բորբոքային հիվանդությունների, ինչպես նաև քաղցկեղի բուժման նպատակով։ 2007թ․-ին ԱՄՆ-ում ամենաշատ վաճառված 20 բեսթ-սելլեր բիոտեխնոլոգիական դեղերից 8-ը թերապևտիկ մոնոկլոնալ հակամարմիններ էին[34]։ Մոնոկլոնալ հակամարմինների արտադրության պահանջարկի այս արագ աճը լավ ազդեցություն թողեց mAb արտադրության ինդուստրիայի վրա[35]։
Տես նաև
խմբագրելԾանոթագրություններ
խմբագրել- ↑ 1,0 1,1 Waldmann TA (March 2003). «Immunotherapy: past, present and future». Nature Medicine. 9 (3): 269–77. doi:10.1038/nm0303-269. PMID 12612576.
- ↑ 2,0 2,1 Sharma P, Allison JP (April 2015). «The future of immune checkpoint therapy». Science. 348 (6230): 56–61. Bibcode:2015Sci...348...56S. doi:10.1126/science.aaa8172. PMID 25838373.
- ↑ Olinger GG, Pettitt J, Kim D, Working C, Bohorov O, Bratcher B, Hiatt E, Hume SD, Johnson AK, Morton J, Pauly M, Whaley KJ, Lear CM, Biggins JE, Scully C, Hensley L, Zeitlin L (October 2012). «Delayed treatment of Ebola virus infection with plant-derived monoclonal antibodies provides protection in rhesus macaques». Proceedings of the National Academy of Sciences of the United States of America. 109 (44): 18030–5. Bibcode:2012PNAS..10918030O. doi:10.1073/pnas.1213709109. PMC 3497800. PMID 23071322.
- ↑ Janeway, Charles; Paul Travers; Mark Walport; Mark Shlomchik (2001). Immunobiology; Fifth Edition. New York and London: Garland Science. ISBN 978-0-8153-4101-7.
- ↑ 5,0 5,1 Janeway CA, Jr.; և այլք: (2005). Immunobiology (6th ed.). Garland Science. ISBN 978-0-443-07310-6.
- ↑ 6,0 6,1 Baxter, David (December 2007). «Active and passive immunity, vaccine types, excipients and licensing». Occupational Medicine. 57 (8): 552–6. doi:10.1093/occmed/kqm110. PMID 18045976.
- ↑ Modified from Carter P (November 2001). «Improving the efficacy of antibody-based cancer therapies». Nature Reviews. Cancer. 1 (2): 118–29. doi:10.1038/35101072. PMID 11905803.
- ↑ Prof FC Breedveld (2000). «Therapeutic monoclonal antibodies». Lancet. 355 (9205): 735–740. doi:10.1016/S0140-6736(00)01034-5. PMID 10703815.
- ↑ Köhler G, Milstein C (August 1975). «Continuous cultures of fused cells secreting antibody of predefined specificity». Nature. 256 (5517): 495–7. Bibcode:1975Natur.256..495K. doi:10.1038/256495a0. PMID 1172191.
- ↑ Ritz J, Schlossman SF (January 1982). «Utilization of monoclonal antibodies in the treatment of leukemia and lymphoma». Blood. 59 (1): 1–11. doi:10.1182/blood.V59.1.1.1. PMID 7032624.
- ↑ Nadler LM, Stashenko P, Hardy R, Kaplan WD, Button LN, Kufe DW, Antman KH, Schlossman SF (September 1980). «Serotherapy of a patient with a monoclonal antibody directed against a human lymphoma-associated antigen». Cancer Research. 40 (9): 3147–54. PMID 7427932.
- ↑ 12,0 12,1 12,2 Stern M, Herrmann R (April 2005). «Overview of monoclonal antibodies in cancer therapy: present and promise». Critical Reviews in Oncology/Hematology. 54 (1): 11–29. doi:10.1016/j.critrevonc.2004.10.011. PMID 15780905.
- ↑ 13,0 13,1 13,2 Hudson PJ, Souriau C (January 2003). «Engineered antibodies». Nature Medicine. 9 (1): 129–34. doi:10.1038/nm0103-129. PMID 12514726.
- ↑ Carter P, Presta L, Gorman CM, Ridgway JB, Henner D, Wong WL, Rowland AM, Kotts C, Carver ME, Shepard HM (May 1992). «Humanization of an anti-p185HER2 antibody for human cancer therapy». Proceedings of the National Academy of Sciences of the United States of America. 89 (10): 4285–9. Bibcode:1992PNAS...89.4285C. doi:10.1073/pnas.89.10.4285. PMC 49066. PMID 1350088.
- ↑ Presta LG, Lahr SJ, Shields RL, Porter JP, Gorman CM, Fendly BM, Jardieu PM (September 1993). «Humanization of an antibody directed against IgE». Journal of Immunology. 151 (5): 2623–32. PMID 8360482.
- ↑ Chothia C, Lesk AM, Tramontano A, Levitt M, Smith-Gill SJ, Air G, Sheriff S, Padlan EA, Davies D, Tulip WR (1989). «Conformations of immunoglobulin hypervariable regions». Nature. 342 (6252): 877–83. Bibcode:1989Natur.342..877C. doi:10.1038/342877a0. PMID 2687698.
- ↑ Jefferis R, Lefranc MP (July–August 2009). «Human immunoglobulin allotypes: possible implications for immunogenicity». mAbs. 1 (4): 332–8. doi:10.4161/mabs.1.4.9122. PMC 2726606. PMID 20073133.
- ↑ Chapman K, Pullen N, Coney L, Dempster M, Andrews L, Bajramovic J, Baldrick P, Buckley L, Jacobs A, Hale G, Green C, Ragan I, Robinson V (2009). «Preclinical development of monoclonal antibodies: considerations for the use of non-human primates». mAbs. 1 (5): 505–16. doi:10.4161/mabs.1.5.9676. PMC 2759500. PMID 20065651.
- ↑ Vennepureddy A, Singh P, Rastogi R, Atallah JP, Terjanian T (June 2016). «Evolution of ramucirumab in the treatment of cancer - A review of literature». Journal of Oncology Pharmacy Practice. 23 (7): 525–539. doi:10.1177/1078155216655474. PMID 27306885.
- ↑ de Zwart, Verena; Gouw, Samantha C; Meyer-Wentrup, Friederike AG (2016 թ․ հունվարի 19). «Antibody therapies for lymphoma in children». Cochrane Database of Systematic Reviews (1): CD011181. doi:10.1002/14651858.cd011181.pub2. ISSN 1465-1858. PMID 26784573.
- ↑ 21,0 21,1 Rang, H. P. (2003). Pharmacology. Edinburgh: Churchill Livingstone. էջ 241. ISBN 978-0-443-07145-4.
- ↑ 22,0 22,1 Pul, Refik; Dodel, Richard; Stangel, Martin (March 2011). «Antibody-based therapy in Alzheimer's disease». Expert Opinion on Biological Therapy. 11 (3): 343–357. doi:10.1517/14712598.2011.552884. PMID 21261567.
- ↑ 23,0 23,1 23,2 23,3 van Dyck, Christopher (2017 թ․ օգոստոսի 24). «Anti-Amyloid-β Monoclonal Antibodies for Alzheimer's Disease: Pitfalls and Promise». Biological Psychiatry. 83 (4): 311–319. doi:10.1016/j.biopsych.2017.08.010. PMC 5767539. PMID 28967385.
- ↑ 24,0 24,1 24,2 24,3 24,4 Panza, F.; Imbimbo, B. P.; Logroscino, G. (2014). «Amyloid-directed monoclonal antibodies for the treatment of Alzheimer's disease: The point of no return?». Expert Opinion on Biological Therapy. 14 (10): 1465–76. doi:10.1517/14712598.2014.935332. PMID 24981190.
- ↑ Hanan, Eilat; Solomon, Beka (January 1996). «Inhibitory effect of monoclonal antibodies on Alzheimer's P-amyloid peptide aggregation». Amyloid. 2 (3): 130–133. doi:10.3109/13506129609014365.
- ↑ Goel, Ayush. «Vasogenic cerebral oedema». radiopaedia.org (անգլերեն). Վերցված է 2017 թ․ նոյեմբերի 1-ին.
- ↑ 27,0 27,1 Panza, F.; Imbimbo, B.P.; D'aOnofrio, G.; Pietrarossa, G.; Seripa, Davide; Frisardi, V. (November 2010). «Bapineuzumab: anti-β-amyloid monoclonal antibodies for the treatment of Alzheimer's disease». V. 2 (6): 767–82. doi:10.2217/imt.10.80. PMID 21091109.
- ↑ Francis RJ, Sharma SK, Springer C, Green AJ, Hope-Stone LD, Sena L, Martin J, Adamson KL, Robbins A, Gumbrell L, O'Malley D, Tsiompanou E, Shahbakhti H, Webley S, Hochhauser D, Hilson AJ, Blakey D, Begent RH (September 2002). «A phase I trial of antibody directed enzyme prodrug therapy (ADEPT) in patients with advanced colorectal carcinoma or other CEA producing tumours». British Journal of Cancer. 87 (6): 600–7. doi:10.1038/sj.bjc.6600517. PMC 2364249. PMID 12237768.
- ↑ Krauss WC, Park JW, Kirpotin DB, Hong K, Benz CC (2000). «Emerging antibody-based HER2 (ErbB-2/neu) therapeutics». Breast Disease. 11: 113–24. doi:10.3233/bd-1999-11110. PMID 15687597.
- ↑ Joyce JA, Fearon DT (April 2015). «T cell exclusion, immune privilege, and the tumor microenvironment». Science. 348 (6230): 74–80. Bibcode:2015Sci...348...74J. doi:10.1126/science.aaa6204. PMID 25838376.
- ↑ Hooks MA, Wade CS, Millikan WJ (1991). «Muromonab CD-3: a review of its pharmacology, pharmacokinetics, and clinical use in transplantation». Pharmacotherapy. 11 (1): 26–37. doi:10.1002/j.1875-9114.1991.tb03595.x (inactive 2020 թ․ մայիսի 21). PMID 1902291.
{{cite journal}}: CS1 սպաս․ DOI inactive as of 2020 (link) - ↑ Chames P, Baty D (2009). «Bispecific antibodies for cancer therapy: the light at the end of the tunnel?». mAbs. 1 (6): 539–47. doi:10.4161/mabs.1.6.10015. PMC 2791310. PMID 20073127.
- ↑ Linke, Rolf; Klein, Anke; Seimetz, Diane (2010). «Catumaxomab: Clinical development and future directions». mAbs. 2 (2): 129–136. doi:10.4161/mabs.2.2.11221. PMC 2840231. PMID 20190561.
- ↑ Scolnik PA (2009). «mAbs: a business perspective». mAbs. 1 (2): 179–84. doi:10.4161/mabs.1.2.7736. PMC 2725420. PMID 20061824.
- ↑ Kelley B (2009). «Industrialization of mAb production technology: the bioprocessing industry at a crossroads». mAbs. 1 (5): 443–52. doi:10.4161/mabs.1.5.9448. PMC 2759494. PMID 20065641.