Մալոնաթթու
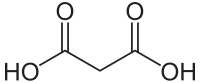
Մալոնաթթու՝ НООС-СН2-СООН, սահմանային երկհիմն կարբոնաթթու, հայտնաբերվել է շաղգամի հյութում։
| Մալոնաթթու | |
|---|---|
 | |
| Ընդհանուր տեղեկություններ | |
| Դասական անվանակարգում | մալոնաթթու |
| Քիմիական բանաձև | C₃H₄O₄ |
| Մոլային զանգված | 1,7E−25 կիլոգրամ[1] գ/մոլ |
| Խտություն | 1,6305 գ/սմ³ գ/սմ³ |
| Ջերմային հատկություններ | |
| Հալման ջերմաստիճան | 135,6 °C °C |
| Տրոհման ջերմաստիճան | 140-160 °C °C |
| Քիմիական հատկություններ | |
| Լուծելիությունը ջրում | 73,5 գ/100 մլ |
| pKa | 1,40×10−3; 2,07×10−6 |
| Դասակարգում | |
| CAS համար | 141-82-2 |
| PubChem | 867 |
| EINECS համար | 205-503-0 |
| SMILES | C(C(=O)O)C(=O)O |
| ЕС | 205-503-0 |
| ChEBI | 844 |
| Եթե հատուկ նշված չէ, ապա բոլոր արժեքները բերված են ստանդարտ պայմանների համար (25 °C, 100 կՊա) | |
Մալոնաթթվի աղերը և էսթերները անվանում են մալոնատներ։
Ֆիզիկական և քիմիական հատկություններ խմբագրել
Մալոնաթթուն լավ լուծվում է ջրում և էթանոլում։ Բենզոլում չի լուծվում։
Մալոնաթթուն հալման կետից քիչ բարձր ջերմաստիճանում տաքացնելիս անջատվում է CO2 և փոխարկվում քացախաթթվի։
Նույն ձևով ալկիլմալոնաթթուները հալաման կետից բարձր ջերմաստիճանում տաքացնելիս կորցնելով CO2 փոխարկվում են ալկիլքացախաթթու, այսինքն՝ պրոպիոնաթթու։
Մեթիլէթիլմալոնաթթուն փոխարկվում է մեթիլէթիլքացախաթթվի, այսինքն՝ վալերիանաթթվի իզոմերներից մեկի։
Ստացում և կիրառում խմբագրել
Սինթետիկ եղանակով մալոնաթթու ստանալու համար քացախաթթվի մոլեկուլում եղած ջրածնի ատոմներից մեկը տեղակալում են քլորով և ստանում քլորքացախաթթու։ Վերջինս փոխազդեցության մեջ դնելով կալիումի ցիանիդի հետ ստանում են ցիանքացախաթթու, որը օճառացումից հետո վերածվում է մալոնաթթվի՝
Մալոնաթթուն կիրառվում է չհագեցած թթուների, ամինաթթուների, վիտամիններ B1 և B6 սինթեզում։
Գրականություն խմբագրել
- Օրգանական քիմիայի դասընթաց, Բ. Ա. Պավլով և Ա. Պ. Տերենտև
- Кнунянц И. Л. и др. т.2 Даффа-Меди // Химическая энциклопедия. — М.: Советская энциклопедия, 1990. — 671 с. — 100 000 экз. — ISBN 5-85270-035-5
Ծանոթագրություններ խմբագրել
Արտաքին հղումներ խմբագրել
- pH-Spectrum of Disodium Malonate Արխիվացված 2012-01-28 Wayback Machine
- pH-Spectrum of Malonate-copper-complex Արխիվացված 2016-03-13 Wayback Machine
- Calculator: Water and solute activities in aqueous malonic acid
| Վիքիպահեստն ունի նյութեր, որոնք վերաբերում են «Մալոնաթթու» հոդվածին։ |