Պարբերություն (քիմիա)
Պարբերություն, քիմիական տարրերի պարբերական համակարգի շարքը, որտեղ ատոմները դասավորված են ըստ միջուկի լիցքի աճման և էլեկտրոններով արտաքին էլեկտրական թաղանթի լրացման։
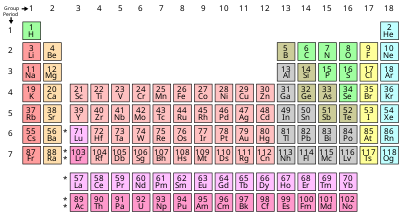
Պարբերական համակարգը կազմված է յոթ պարբերություններից։ Առաջին պարբերությունում առկա է երկու քիմական տարր, իսկ երկրորդում և երրորդում՝ ութական։ Այս երեք պարբերությունները կոչվում են փոքր պարբերություններ։ Մյուս պարբերությունները, որոնցում առկա են 18 և ավելի տարրեր, կոչվում են մեծ պարբերություններ։ Պարբերության համարով որոշվում է տարրում էլեկտրոնային թաղանթների քանակը (էներգիական մակարդակներ)։
Յուրաքանչյուր պարբերություն (բացի առաջինից) սկսվում է ալկալիական մետաղով (Li, Nа, К, Rb, Cs, Fr) և ավարտվում ազնիվ գազով (Ne, Ar, Kr, Хе, Rn, Og), որին նախորդում է ոչ մետաղ։
Առաջին պարբերությունում, բացի հելիումից[1][2][3][4][5], կա մեկ տարր՝ ջրածինը[6][7], որն ունի ինչպես մետաղներին, այնպես էլ (ավելի շատ) ոչ մետաղներին բնորոշ հատկություններ։ Այս տարրերի մոտ էլեկտրոններով լրացվում է 1s-ենթամակարդակը։
Երկրորդ և երրորդ պարբերությունների տարրերի մոտ լրացվում են s- և р-ենթամակարդակները։ Փոքր պարբերությունների տարրերին բնորոշ է էլեկտրաբացասականության կտրուկ աճ միջուկի լիցքի աճմանը զուգընթաց, թուլանում են մետաղական և ուժեղանում ոչ մետաղական հատկությունները։
Չորրորդ և հինգերորդ պարբերությունները ներառում են անցումային d-տարրեր (սկանդիումից մինչև ցինկ և իտրիումից կադմիում), որոնց մոտ էլեկտրոններով արտաքին s-ենթամակարդակի լրացումից հետո, համաձայն Կլեչկովսկու օրենքի, լրացվում է նախորդ էլեկտրոնային մակարդակի d-ենթամակարդակը։
1s
2s 2p
3s 3p
4s 3d 4p
5s 4d 5p
6s 4f 5d 6p
7s 5f 6d 7p
6f 7d 7f
...
Վեցերորդ և յոթերորդ պարբերություններում լրացվում են 4f- և 5f-ենթամակարդակները, որոնք պարունակում են 14 տարրով ավելի, քան չորրորդ և հինգերորդ պարբերությունները (լանթանիդները վեցերորդ և ակտինիդները յոթերորդ պարբերություններում)։
Հետագայում պարբերությունները տարբերակվել են ըստ երկարության կամ այլ հատկանիշի, ինչի շնորհիվ պարբերական համակարգում դրանց տեղակայման տարբեր եղանակներ։ Պարբերական համակարգի կարճ ձևում փոքր պարբերություններն ունեն մեկական շարք, իսկ մեծ պարբերությունները՝ երկու։ Պարբերական համակարգի երկար ձևում բոլոր պարբերությունները կազմված են մեկ շարքից։
| Տարրերի քանակ | 2 կամ 8 | 18 և ավելի |
| Էլեկտրոնների բաշխում | լրացնում են միայն s- և р-ենթամակարդակները | լրացնում են նաև նախավերջին d-ենթամակարդակը և նախանախավերջին f-ենթամակարդակը |
| Տարրերի հատկությունների փոփոխություն | մետաղական հատկություններն արագ թուլանում են | դանդաղ անցում մետաղական հատկություններից ոչ մետաղական հատկությունների |
Մեկ պարբերությունում ներառված տարրերն ունեն մոտ հարաբերական ատոմային զանգված, սակայն տարբեր ֆիզիկական և քիմիական հատկություններ, ի տարբերություն նույն խմբի տարրերի։ Կարգաթվի աճմանը զուգընթաց պարբերություններում փոքրանում է ատոմի շառավիղը և աճում վալենտային էլեկտրոնների թիվը, ինչի հետևանքով տեղի է ունենում տարրերի մետաղական հատկությունների թուլացում և նրանց ոչ մետաղական հատկությունների ուժեղացում, թուլանում են տարրերի և նրանց միացությունների վերականգնիչ և ուժեղանում օքսիդիչ հատկությունները։
Ծանոթագրություններ
խմբագրել- ↑ «Helium: physical properties». WebElements. Վերցված է 2008 թ․ հուլիսի 15-ին.
- ↑ «Helium: geological information». WebElements. Վերցված է 2008 թ․ հուլիսի 15-ին.
- ↑ Cox, Tony (1990 թ․ փետրվարի 3). «Origin of the chemical elements». New Scientist. Վերցված է 2008 թ․ հուլիսի 15-ին.
- ↑ «Helium supply deflated: production shortages mean some industries and partygoers must squeak by». Houston Chronicle. 2006 թ․ նոյեմբերի 5.
- ↑ Brown, David (2008 թ․ փետրվարի 2). «Helium a New Target in New Mexico». American Association of Petroleum Geologists. Վերցված է 2008 թ․ հուլիսի 15-ին.
- ↑ Palmer, David (1997 թ․ նոյեմբերի 13). «Hydrogen in the Universe». NASA. Վերցված է 2008 թ․ փետրվարի 5-ին.
- ↑ Jolly, William Lee (2019 թ․ օգոստոսի 9). «hydrogen». Encyclopædia Britannica.