Կարբոնիլային միացություններ
| Այս հոդվածն աղբյուրների կարիք ունի։ Դուք կարող եք բարելավել հոդվածը՝ գտնելով բերված տեղեկությունների հաստատումը վստահելի աղբյուրներում և ավելացնելով դրանց հղումները հոդվածին։ Անհիմն հղումները ենթակա են հեռացման։ |
Կարբոնիլ խումբ պարունակող միացությունները կախված կարբոնիլ խմբի հետ կապված տեղակալիչների բնույթից բաժանվում են մի շարք դասերի՝ ալդեհիդների, կետոնների, կարբոնաթթուների և կարբոնաթթուների ածանցյալների։
| Դասի միացությունները | Կառուցվածք | Ընդհանուր բանաձևերը |
|---|---|---|
| Ալդեհիդներ | 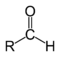
|
|
| Կետոններ | 
|
|
| Բարդ եթերներ | 
|
|
| Ամիդներ | 
|
|
| Հալոգենանհիդրիդ | 
|
|
| Կարբոնաթթուներ | ||
| Կարբոնաթթվի անհիդրիդ | 
|
Ալդեհիդներ և կետոններ
խմբագրելԱլդեհիդներում և կետոններում կարբոնիլային խումբը կապված է ալկիլ կամ արիլ ռադիկալների (ալդեհիդներում նաև ջրածնի) հետ։
Ալդեհիդների առաջացման եղանակները
խմբագրել- 1.Ալդեհիդները և կետոնները առաջանում են համապատասխանաբար առաջնային և երկրորդային սպիրտների օքսիդացումից։
R-CH2OH→R-CHO
R-CH(OH)-R→R-CO-R
Կենսաբանական համակարգերում օքսիդացումը կատարվում է ֆերմենտատիվ եղանակներով (NAD և FAD պարունակող դեհիդրոգենազներով, օքսիդազներով)։
- 2.Հեմ դիհալոգենիդների հիդրոլիզից։
- 3.Կարբոնաթթուների որոշ ածանցյալների վերականգնումից առաջանում են ալդեհիդներ։ Օրինակ, կարբոնաթթուների քլորանհիդրիդներից (պալադիումի ներկայությամբ՝ Ռոզենմունդի ռեակցիա)։
- 4.Երկարժեք սնդիկի (Hg2+) աղերի ներկայությամբ (Կուչերովի ռեակցիա) ալկինների հիդրատացման դեպքում առաջանում են ալդեհիդներ և կետոններ։
HC≡CH+H2Օ→CH3-CHO
CH3-C≡CH+H2O→CH3-CO-CH3
Ալդեհիդների և կետոնների քիմիական հատկությունները
խմբագրելՔիմիական հատկությունները պայմանավորված են կարբոնիլային միացությունների մոլեկուլներում ռեակցիոն կենտրոնների բնույթով։
Ալդեհիդների և կետոնների տված ռեակցիաները, կախված ռեագենտի բնույթից, բաժանվում են հիմնական երեք խմբի՝
- 1.փոխազդեցություն նուկլեոֆիլների հետ (նուկլեոֆիլ միացման ռեակցիաներ)
- 2.ալդոլ միացման ռեակցիաներ
- 3.օքսիդավերականգնման ռեակցիաներ։
Փոխազդեցությունը նուկլեոֆիլների հետ
խմբագրելԿարբոնիլ խումբ պարունկաող միացությունների փոխազդեցությունը նուկլեոֆիլների հետ կատարվում է միացման կամ կոնդեսացման (ջրի կամ սպիրտի անջատումով) եղանակներով։ Ռեակցիայի առաջին փուլում կատարվում է նուկլեոֆիլ գրոհ կարբոնիլ խմբի ածխածնի վրա։ Այս փուլը ընդհանուր է նշված երկու եղանակների համար։H-X կառուցվածքի միացության փոխազդեցությունը կարբոնիլ խմբի հետ կատարվում է հետևյալ մեխանիզմով։
RR’C=O→RR’C(O-)X-H→RR’C(OH)X
Կարբոնիլ խմբի բևեռացման հետևանքով ածխածնի ատոմի վրա գոյանում է մասնակի դրական լիցք, իսկ թթվածնի ատոմի՝ մասնակի բացասական լիցք։ Ռեագենտ H-X-ի X նուկլեաֆիլ խումբը տրամադրում է կարբոնիլ խմբի ածխածնին էլեկտրոնային զույգ։ Սկզբից տեղի է ունենում ավելի էֆեկտիվ (X-) նուկլեաֆիլի գրոհը ածխածնի ատոմի վրա, որից հետո պրոտոնը միանում է թթվածնին։ Որոշ դեպքերում ռեակցիայի արագության մեծացման նպատակով օգտագործում են թթվային կատալիզատորներ.պրոտոնը միանում է կարբոնիլ խմբի հիմնային կենտրոնի թթվածնին, որի հետևանքով ածխածնի մասնակի դրական լիցքը վերածվում է լրիվ լիցքի և առաջին փուլում սուբստրատի մոլեկուլը վերածվում է դրական լիցքավորված իոնի, կարբկատիոնի։ Կարբկատիոնի անկայունության հետևանքով առաջին փուլը դարձելի է։ Հաջորդ փուլում կատարվում է նուկլեաֆիլի գրոհը։ Բոլոր այն գործոնները, որոնք մեծացնում են մասնակի դրական լիցքը կարբոնիլ խմբի ածխածնի ատոմի վրա մեծացնում են նուկլեաֆիլի գրոհի հնարավորությունը։ Էլեկտրաակցեպտոր բնույթի տեղակալիչները ռադիկալում նպաստում են ռեակցիոնունակության աճին, սակայն ի տարբերություն էլեկտրադոնոր տեղակալիչների։
CH3CHO < H-CHO < Cl3C-CHO
Ձախից աջ ռեակցիոնունակությունը աճում է։
Ալդեհիդի և սպիրտի փոխազդեցությունից առաջանում են կիսաացետալներ։ Թթվային կատալիզատորի ներկայությամբ կիսաացետալները շարունակում են փոխազդել սպիրտի հետ, առաջացնելով ացետալներ-դիոլների դիալկիլ եթեր։
Կիսաացետալների առաջացումը։
Ացետալների առաջացման մեխանիզմը։ Ռեակցիան ընթանում է թթվային կատալիզատորի ներկայությամբ։ Պրոցեսի բոլոր ռեակցիաները դարձելի են։
Եթե տվյալ միացության մոլեկուլում կան ալդեհիդային և սպիրտային խմբեր, ապա հնարավոր է ցիկլիկ կիսաացետալների առաջացում։ Այս դեպքում ցիկլիկ ձևը ավելի կայուն է, հատկապես, երբ առաջացած ցիկլը 5 կամ 6 անդամանի է։
Կենդանի օրգանիզմներում մեծ թվով միացություններ, այդ թվում մոնոսախարիդները, գտնվում են ցիկլիկ կիսաացետալների ձևով։
Թթվային միջավայրում ացետալները հիդրոլիզվում են մինչև կիսաացետալներ, ապա մինչև ալդեհիդ և սպիրտ։ Հիմնային միջավայրում հիդրոլիզ տեղի չի ունենում, քանի որ ալկօքսիդ խումբը ավելի վատ հեռացող խումբ է, քան հիդրօքսիդ խումբը։
Ջրի հետ փոխազդելիս կարբոնիլային միացությունները առաջացնում են հիդրատներ, որոնք անկայուն միացություններ են և գոյություն ունեն միայն ջրային լուծույթներում։ Թորման եղանակով անջատելու փորձերը ապարդյուն են՝ հիդրատները վերածվում են ելանյութերի՝ ալդեհիդի և ջրի։
Աղյուսակ.Ալդեհիդների և կետոնների նուկլեաֆիլ միացման մեխանիզմով ընթացող հիմնական ռեակցիաները
| H-X | ալդեհիդ կամ կետոն | Ռեակցիայի արդյունքը |
|---|---|---|
| H-C≡N | +RR’C=O | RR’C(OH)CN-ցիանոհիդրին |
| H-NH2 | +RR’C=O | RR’C(OH)NH2-ալդեհիդոամիակ |
| H-OH | +RR’C=O | RR’C(OH)OH-հեմ-դիոլ |
| H-O-R" | +RR’C=O | RR’C(OH)OR"-կիսաացետալ |
| H-S-R" | +RR’C=O | RR’C(OH)SR"-կիսաացետալ |
| R,R'=ալկիլ կամ H |
Ռեակցիայի հավասարակշռային վիճակը պայմանավորված է ելանյութերի ռադիկալների կառուցվածքով՝ ֆորմալդեհիդի հիդրատային ձևը կազմում է 99.99 %,ացետալդեհիդինը՝ 58. %,ացետոնի հիդրատային ձևը չնչին է։
Էլեկտրաակցեպտոր տեղակալիչների ներմուծումը ռադիկալ նպաստում է հիդրատային ձևերի կայունացմանը։ Օրինակ, քլորալի հիդրատային ձևը, քլորալհիդրատը, որը օգտագործվում է բժշկության մեջ, որպես հանգստացնող և քնաբեր դեղանյութ, գոյություն ունի առանձին միացության ձևով։
Քլորալհիդրատի դեհիդրատացումը կատարվում է խիստ պայմաններում, խիտ ծծմբական թթվի ներկայությամբ։ Նուկլեաֆիլ միացման ռեակցիաների ժամանակ կարբոնիլ խմբի հարթ sp2 հիբրիդացման վիճակում գտնվող ածխածնի ատոմը անցնում է քառանիստ sp3 հիբրիդային վիճակի, տեղակալիչների ավելի «խիտ» են դասավորվում ածխածնի ատոմի շուրջ և նրանց բնույթը (ծավալը, մեծությունը) այս պայմաններում, ունի որոշիչ նշանակություն ռեակցիոնունակության համար.ծավալուն էլեկտրադոնոր տեղակալիչների դեպքում ռեակցիոնունակությունը նվազում է։ Նշանակում է, որ ալդեհիդները ավելի ռեակցիոնունակ են, քան կետոնները։
Կոնդեսացման ռեակցիաները տեղի են ունենում NH2-խումբ պարունակող բազմաթիվ օրգանական միացությունների հետ։
Ռեակցիայի մեխանիզմը հետևյալն է՝ առաջին փուլում H2N-Y միացությունը վերը նկարագրված նուկլեաֆիլ միացման մեխանիզմով միանում է կարբոնիլ խմբին։ Թույլ թթվային միջավայրում (օրինակ, ացետատային բուֆերի դեպքում,pH=4,5) հիդրօքսիլ խմբի թթվածինը պրոտոնացվում է, որից հետո անջատվում է ջուր և, ապա պրոտոն։
Առաջացած իմինները հիդրոլիզվում են առաջացնելով ալդեհիդներ և կետոններ։ Կախված համապատասխան ռադիկալների բնույթից հիդրոլիզի ենթարկվելու հավանականությունը նվազում է՝
R(H>Alk>Ar)
Վերջինների դեպքում անհրաժեշտ է կատալիզատոր։
Աղյուսակ.Ալդեհիդների և կետոնների կոնդեսացման մեխանիզմով ընթացող հիմնական ռեակցիաները և արդյունքները
| H2N-Y | ալդեհիդ կամ կետոն | ռեակցիայի արդյունքը |
|---|---|---|
| H2N-Y | +RR’C=O | RR1C=N-R-իմին (եթե R կամ R'Ar-Շիֆի հիմք) |
| H2N-OH | +RR’C=O | RR1C=N-OH-օքսիմ |
| H2N-NH2 | +RR’C=O | RR1C=N-NH2- հիդրազոն |
| H2N-NH-C6H5 | +RR’C=O | RR1C=N-NH-C6H5-ֆենիլհիդրազոն |
Ալդեհիդների և կետոնների կետո-ենոլ տաուտոմերիա.ալդոլ միացում
խմբագրելՀիմնային միջավայրում կարբոնիլ խմբի հարևան ածխածնի ատոմից պրոտոնի արագ անջատման շնորհիվ առաջանում է անիոն (CH-թթվայնություն)։ Պրոցեսը կատարվում է արագ, շնորհիվ կարբոնիլ խմբի էլեկտրաակցեպտորային էֆեկտի և առաջացած մեզոմեր կառուցվածք ունեցող ենոլյատ-անիոնի կայունության (անիոնում բացասական լիցքը ապատեղայնացված է)։
Առաջացած ենոլյատ-անիոնը կարող է պրոտոնացվել իր երկու սահմանային դիրքերով, իզոմերների, կամ տաուտոմերների (կետո և ենոլ ձևերի) առաջացումով։
Տաուտոմերիան բնորոշ է «շարժուն» ջրածնի ատոմ ունեցող միացություններին։
CH3-CH2-CH=O→CH3CH=CH-OH
CH3-CH2-CO-CH2-CH3→→CH3-CH=C(OH)-CH2-CH3
Հիմքերի և թթուների կատալիտիկ քանակների ներկայությամբ ալդեհիդները և կետոնները առաջացնում են դիմերներ։ Այդ ռեակցիաները կոչվում են ալդոլ միացման ռեակցիաներ և կատարվում միջանկյալ ենոլյատ-անիոնի առաջացումով, որը հանդես է գալիս որպես նուկլեաֆիլ և գրոհում ալդեհիդի կամ կետոնի հաջորդ մոլեկուլի կարբոնիլ խմբի վրա։
2CH3-CH=O+NaOHլ-թ→CH3-CH(OH)-CH2-CH=O
Տվյալ պրոցեսի բոլոր ռեակցիաները դարձելի են, և սովորաբար, միջավայրում գտնվում է ելանյութերի և ալդոլի հավասարակշիռ խառնուրդ։ Ավելի խիստ պայմաններում, թթվային կատալիզատորի ներկայությամբ տեղի է ունենում կրոտոնային կոնդեսացում, անջատվում է ջուր և առաջանում է α,β-չհագեցած կարբոնիլային միացություն։
R-CH2-CH(OH)-CH(R)-CH=O→R-CH2-CH=C(R)-CH=O
Կենսաբանական համակարգերում ալդոլային միացման եղանակով կատարվում են բազմաթիվ ռեակցիաներ՝ կիտրոնաթթվի սինթեզը, գլյուկոզ-1,6-դիֆոսֆատի առաջացումը ածխաջրերի նյութափոխանակության ժամանակ, երբ երկու տրիոզֆոսֆատներից (ֆոսֆոգլիցերատից և ֆոսֆոդիօքսիացետոնից) առաջանում է հեքսոզդիֆոսֆատ (ֆրուկտոզ-1,6-դիֆոսֆատ),որի շնորհիվ օրգանիզմը կարող է ապահովել իրեն գլյուկոզով։ Ռեակցիան կատալիզում է ալդոլազ ֆերմենտով։
Հալոֆորմային ռեակցիա։ Թթուների և հիմքերի ներկայությամբ ալդեհիդները և կետոնները հեշտությամբ փոխազդում են հալոգենների հետ՝ տեղակալելով ռադիկալում մեկ կամ մի քանի ջրածնի ատոմ։ Ալդեհիդների և կետոնների α-հալոգենածանցյալները գրգռում են քթի և աչքերի լորձաթաղանթները (լակրիմատորներ են)։CH3-CO-R տիպի կառուցվածք ունեցող միացությունները հիմնային միջավայրում փոխազդում են, առաջանում է եռհալոգենկարբոնիլային միացություն, որը քայքայվում է հալոֆորմի առաջացումով։ Յոդի հետ ռեակցիան անցկացնելու դեպքում առաջանում է յուրահատուկ հոտ ունեցող միացություն՝ յոդոֆորմ։ Անալիտիկ քիմիայում օգտվում են յոդոֆորմային ռեակցիայից, միացությունների կառուցվածքների պարզաբանման նպատակներով։
Կարբոնիլային միացությունների օքսիդավերականգնման ռեակցիաները
խմբագրելԿարբոնիլային միացությունների վերականգնումը կատարվում է միայն ուժեղ վերականգնիչների (LiAlH4,KBH4) ազդեցության պայմաններում, սպիրտների առաջացումով։
Ալդեհիդների և կետոնների վերականգնման ռեակցիայի մեխանիզմը։ Պրոցեսը նման է կենսաքիմիական համակարգերում գործող մեխանիզմներին, որոնց մասնակցում են NADH որպես կոնֆերմենտ և հիդրիդ-իոնի դոնոր։ Ռեակցիոն խառնուրդում բորհիդրիդը հանդես է գալիս որպես հիդրիդ-իոնի (H-։) դոնոր, պրոցեսը ընթանում է երկու փուլով։ Առաջին փուլում NaBH4-ը կարբոնիլային ածխածնի հետ կովալենտ կապի առաջացմանը տրամադրում է հիդրիդ-իոնը իր երկու էլեկտրոնով.արդյունքնում առաջանում է անիոն։ Ռեակցիան շարունակվում է թթվի ջրային լուծույթում և առաջանում է չեզոք ալկոհոլ։
Ալդեհիդների օքսիդացման արդյունքում, կախված միջավայրի բնույթից առաջանում են տարբեր միացություններ։ Ալդեհիդները, ի տարբերություն կետոնների, հեշտությամբ են օքսիդանում թթվային միջավայրում, վերածվելով համապատասխան կարբոնաթթուների։
α-դիրքում ջրածին չունեցող ալդեհիդները ուժեղ հիմքերի ներկայությամբ տալիս են Կանիցարոյի ռեակցիան՝ ենթարկվում են ինքնաօքսիդացման-ինքնավերականգնման։
ArCHO→Ar-CH2OH+Ar-COONa
2R3C-CHO+NaOH→2R3C-CH2OH+R3C-COONa
Ալդեհիդները օքսիդանում են ինչպես սովորական օքսիդիչների օգնությամբ (քրոմաթթու, կալիումի պերմանգանատ, ազոտական թթու),այնպես էլ թույլ օքսիդիչների ազդեցությամբ՝ արծաթի (I) և պղնձի (II) միացություններով (հիմնային միջավայրում)։ Օրինակ, Ֆելինգի հեղուկը, որը պարունակում է երկարժեք (II) պղինձ և Տոլենսի ռեակտիվը (արծաթի նիտրատի ամոնիակային լուծույթ) օքսիդացվում են ալդեհիդները, առաջացնելով պղնձի օքսիդ (I) և մետաղական արծաթ։ Այդ ռեակցիաները օգտագործում են որպես ալդեհիդների հայտնաբերման ռեակցիաներ։
- RCHO + 2Cu(OH)2 → RCOOH + Cu2O + 2H2O
2Cu++2OH-→Cu2O+H2O
Կետոնների օքսիդացումը կատարվում է դժվարությամբ։ Ռեակցիան ընթանում է ուժեղ օքսիդիչների ներկայությամբ և C-C կապերի քայքայումով։
Առաջանում է կարճ շղթա ունեցող օքսիդացման տարբեր աստիճանի միացությունների խառնուրդ։