Կալիումի քլորատ
Կալիումի քլորատ (Բերթոլեի աղ) — , քլորական թթվի կալիումական աղ։ Անգույն բյուրեղներ, խտությունը՝ 2320 կգ/մ³, հալման ջերմաստիճանը՝ 356° С, թունավոր է, ջրում վատ է լուծվում (մոտ 7,5 գ` 100 գ ջրում, 20 °C–ում)։ Կալիումի քլորատը օքսիդիչ է, ծծմբի, ֆոսֆորի, ածխածնի և օրգանական նյութերի հետ առաջացնում է պայթուցիկ խառնուրդներ։ Ստացվում է -ի ջրային լուծույթի էլեկտրոլիզով։ Օգտագործվում է լուցկու արդյունաբերությունում և պիրոտեխնիկայում, նաև քիմիական աշխատանոցում թթվածին ստանալու համար, իսկ բժշկության մեջ՝ որպես ախտահանիչ։
| Կալիումի քլորատ | |
|---|---|
 | |
 | |
 | |
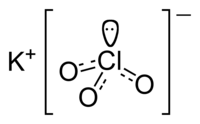
| Քիմիական բանաձև | KCIO₃ |
| Ֆիզիկական հատկություններ | |
| Ագրեգատային վիճակ | անգույն բյուրեղներ |
| Մոլային զանգված | 2,0E−25 կիլոգրամ[1] գ/մոլ |
| Խտություն | 2,32 գ/սմ³ գ/սմ³ |
| Հալման ջերմաստիճան | 356 °C °C |
| Կազմալուծման ջերմաստիճան | 400 °C[2] |
| Գոյացան էնթալպիա | −391,204 կՋ/մոլ կՋ/մոլ |
| Քիմիական հատկություններ | |
| Դասակարգում | |
| CAS համար | 3811-04-9 |
| PubChem | 6426889 |
| EINECS համար | 223-289-7 |
| SMILES | [O-]Cl(=O)=O.[K+] |
| ЕС | 223-289-7 |
| RTECS | FO0350000 |
| ChEBI | 18512 |
| Եթե հատուկ նշված չէ, ապա բոլոր արժեքները բերված են ստանդարտ պայմանների համար (25 °C, 100 կՊա) | |
Պատմություն խմբագրել
Առաջին անգամ ստացվել է 1786 թվականին Կլոդ Բերթոլեի կողմից (այստեղից էլ անվանումը` Բերթոլեի աղ), քլորը, տաք խտացրած կալիումի հիդրօքսիդով անց կացնելով։
Քիմիական հատկություններ խմբագրել
Տաքացնելիս (400°С) քայքայվում է՝ առաջացնելով , ավելի բարձր ջերմաստիճաններում (550- 600°С)՝ կալիումի քլորիդ և թթվածին։
- (400 °C);
- (550—620 °C)
Կատալիզատորների ( ) առկայությամբ քայքայվում է ավելի ցածր ջերմաստիճաններում (200 °C)։
- (150—300 °C, կատ. )
Ջրասպիրտային լուծույթում ռեակցիայի մեջ է մտնում ամոնիումի սուլֆատի հետ, առաջացնելով ամոնիումի քլորատ։
Կիրառում խմբագրել
Այրվող նյութեր խմբագրել
Կալիումի քլորատի խառնուրդները վերականգնիչների հետ (ֆոսֆոր, ծծումբ, օրգանական միացություններ) պայթուցիկ և զգայուն են շփման, հարվածների նկատմամբ։ Զգայունությունը ավելանում է բրոմատների և ամոնիումի աղերի առկայությամբ։ Բերթոլեի աղի հետ բաղադրության բարձր զգայունության պատճառով, նրանք գրեթե չեն օգտագործվում արդյունաբերական և ռազմական պայթուցիկ նյութերի արտադրության համար։ Երբեմն օգտագործվում է հրարվեստում, որպես քլորատի աղբյուր, մտնում է լուցկու գլխիկի այրվող նյութի բաղադրության մեջ։
Բժշկության մեջ խմբագրել
Որոշ ժամանակ կալիումի քլորատի լուծույթները կիրառվում էին թույլ հականեխիչի տեղ, արտաքին դեղամիջոց կոկորդ ողողելու համար։
Թունավորություն խմբագրել
Կալիումի քլորատի մահացու չափը կազմում է 1գ/կգ։
Ծանոթագրություններ խմբագրել
| Այս հոդվածի կամ նրա բաժնի որոշակի հատվածի սկզբնական կամ ներկայիս տարբերակը վերցված է Քրիեյթիվ Քոմմոնս Նշում–Համանման տարածում 3.0 (Creative Commons BY-SA 3.0) ազատ թույլատրագրով թողարկված Հայկական սովետական հանրագիտարանից (հ․ 2, էջ 422)։ |

